
日本語版(English follows)
バイリンガル製薬業界概説について
バイリンガル製薬業界概説では、製薬業界の特有の慣習や仕組みについて、日本語で解説し、それを英語で伝える際のコツを紹介していく。
第4回の今回は医薬品業界人として知っておくべき情報源を分野別に紹介する。
英語版はネイティブスピーカーが朗読した音声付である。
Contents
規制当局ウェブサイト
厚生労働省(MHLW)
言わずと知れた医薬品を規制する日本の当局のウェブサイトである。
薬事・食品衛生審議会関係(部会等)、中央社会保険医療協議会(中医協)関係の資料に加えて、医薬品規制の今後の方向性等を知るために定期的にチェックしておいて損はないサイトである。
また、医薬品の品質規格書である日本薬局方の情報も掲載されている。
なお、日本薬局方のファイルは日英ともに無料で公開されている。
医薬品医療機器総合機構(PMDA)
医薬品に係る具体的な規制情報を収集するうえでは最も重要なウェブサイトである。
PMDAには大きく分けて審査業務、安全対策業務及び健康被害救済業務の3つの業務がある。
このうち医薬品業界で仕事をするうえで主として関係するのは審査業務と安全対策業務である。
審査業務は医薬品の市販前、安全対策業務は医薬品の市販後に主として焦点をあてた業務である。
このウェブサイトからは、承認されている医薬品の添付文書、審査報告書等の文書のダウンロードが可能である。
具体的なダウンロード方法は以下に図示した。
トップページの以下のボタンをクリックする。

次の画面で検索したい医薬品名を入れる。ここではオプジーボをの添付文書と審査報告書を検索する。
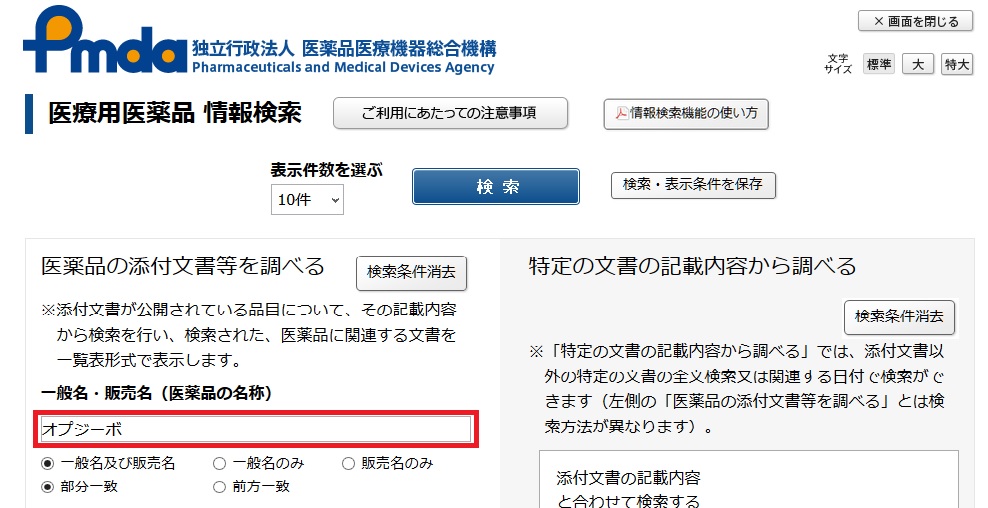
添付文書と審査報告書にcheckが入っていることを確認する。
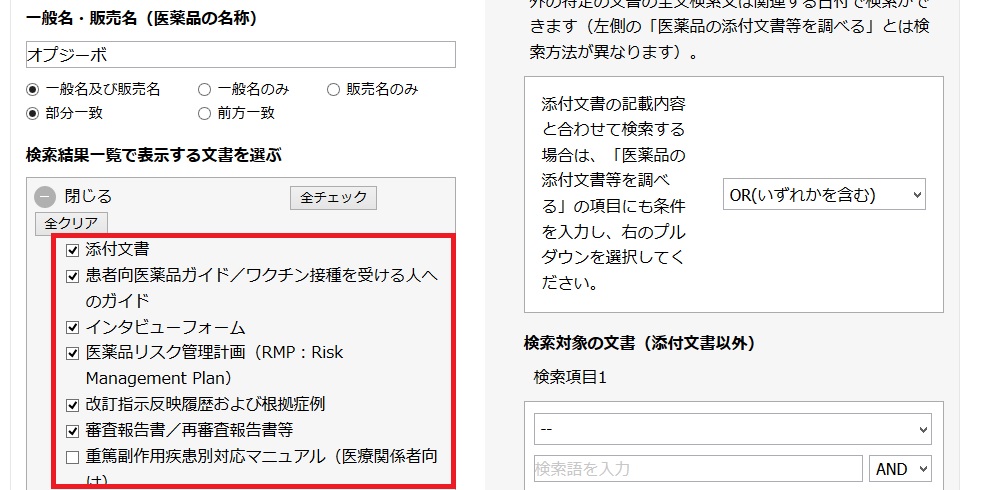
この確認が終ったら、検索ボタンをクリック。
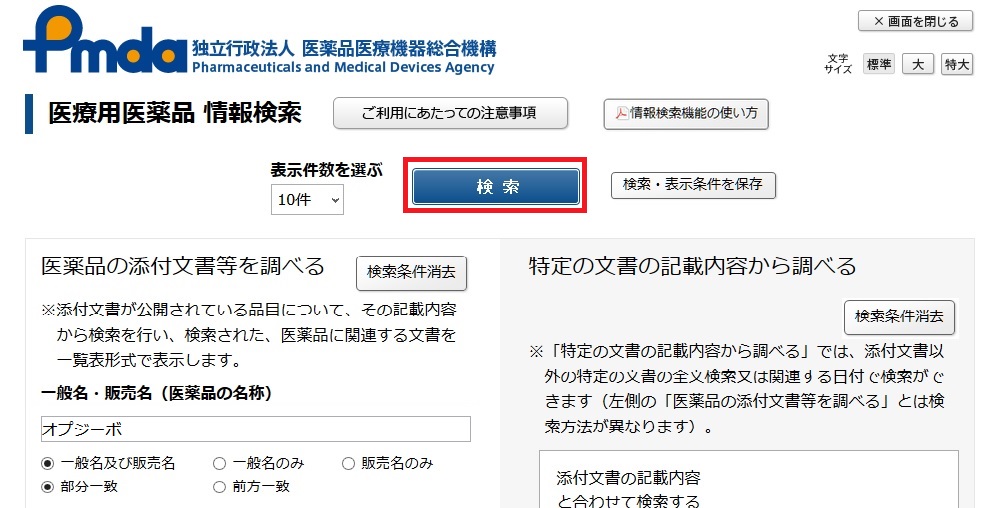
出てきた画面を右にスクロールして添付文書と審査報告書へのリンクをクリックする。
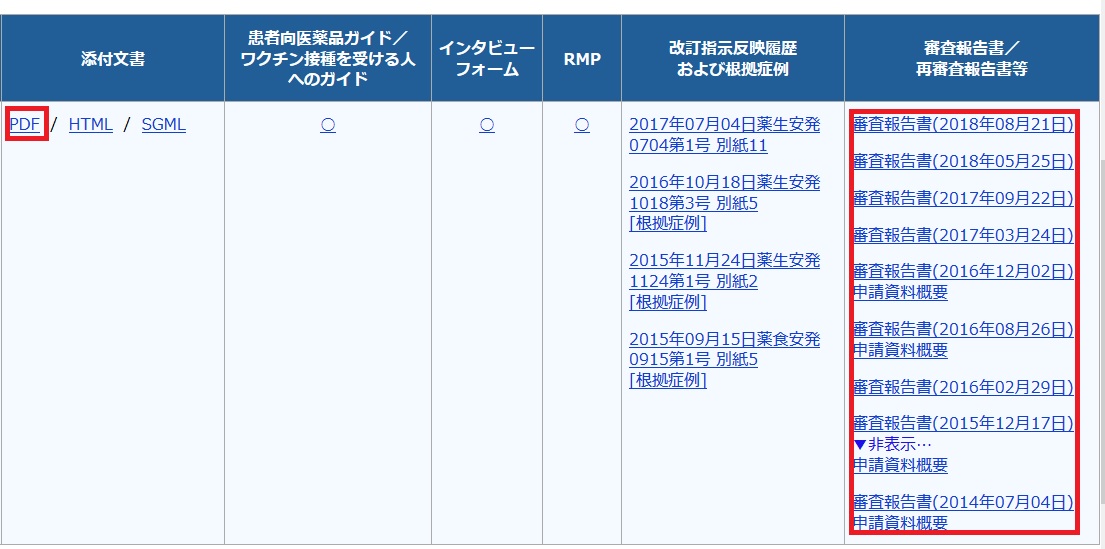
審査報告書の列からは申請資料概要(公開CTD)も閲覧可能である。
US Food and Drug Administration (FDA)
米国食品医薬品局。
言わずと知れた米国の医薬品等規制当局である。
このウェブサイトでは日本のPMDA同様、米国で医薬品等の製品を上市するのに必要な規制・プロセスの情報及び医薬品の審査・安全性情報を得ることができる。
European Medicines Agency (EMA)
欧州医薬品庁。
欧州連合の規制当局である。
このウェブサイトでも日本のPMDA同様、欧州連合で医薬品等の製品を上市するために必要な規制・プロセス及び医薬品の審査・安全性情報を得ることができる。
業界団体ウェブサイト
日本製薬団体連合会(日薬連)
製薬会社の業界団体の団体である。
製薬協等の業種別の団体と関薬協や東薬工などの地域別団体の両方から構成される。
日本製薬工業協会(製薬協)
研究開発志向の製薬会社から構成される業界団体。
日本の薬事行政という医薬品に係る規制をまとめた資料(日英)を毎年更新して無償配布している。
関西医薬品協会(関薬協)
関西地区の製薬会社から構成される業界団体。元々は大阪医薬品協会(大薬協)と呼ばれていた。
医薬品業界はもともと大阪の道修町で発達し関西に本社を置く製薬企業も多かったため、関薬協は東薬工よりも影響力が大きい。
なお、製薬関連団体企業が使用できるpraise-netは、日々発出される規制当局通知のデータベースであり業界人の必須ツールである。
東京医薬品工業協会(東薬工)
東京地区の製薬会社から構成される業界団体。
論文検索ウェブサイト
PubMed
US National Library of Medicine(米国国立医学図書館)が提供する生命科学・医学論文のデータベース。英語論文の調査に使うサイトとしては第一選択になる。
医学中央雑誌(医中誌)
上記PubMedは日本語論文をカバーしていないため、日本語の医学論文を検索する際には、こちらのサイトが第一選択になる。利用するには有料のユーザー登録が必要である。
その他ウェブ情報源
Medical Dictionary for Regulatory Activities (MedDRA)
ICHの活動により共通の規制当局や製薬企業のための共通医学用語辞書のニーズを満たすために開発された。元々は英国の規制当局であるMedicines and Healthcare products Agency(MHRA)の用語集を基盤としている。
本来非営利の目的のために使用するなら無料で利用できるが、日本語翻訳が必要な場合はJapan Maintenance Organizationに登録して有料での使用となる。
書籍
医薬品製造販売指針
業界団体の有志が編纂し、じほうが発行する日本の医薬品に関する規制・必要手続きをほぼすべて網羅する書籍。
業界ニュース
日刊薬業
製造販売指針や治療薬ハンドブックなど業界の人なら誰でも知っている本の出版社であるじほうが発行する日刊ニュース。
基本的に有料であるが無料登録で有料記事が読めるプランもある。
薬事ニュース
週刊の業界ニュース紙。
医療従事者や製薬企業向けのYakuji News-Net Dayは最新のニュースをメールで受け取れたり、薬事食品衛生審議会資料等の速報・データベースが充実している。
ミクス
月刊誌だけあって、ニュース主体でなく、業界のトレンドに関して、病院、薬局、卸、製薬と医薬品業界全般的にバランスよくマーケティングよりの視点で書かれた記事が魅力。
月刊薬事
こちらも日刊薬業と同様じほうが発行する月刊誌。
薬事とあるが病院・薬局勤務の薬剤師によりフォーカスした内容である。
English version(英語版)
About Bilingual Pharma Industry Topics
In this Bilingual Pharma Industry Topic series, pharma-industry specific practices or ways of doing businesses are explained in Japanese, followed by tips for conveying the same info in English.
The forth topic for the series is resources that you should know as a pharma industry person, which is introduced for each category.
Ministry of Health, Labour and Welfare (MHLW)
This is obvious, but it is the Japanese regulatory authority’s website that regulates drugs.
This is a website that you should check regularly to know the trend about drug regulations.
Materials about Pharmaceutical Affairs and Food Sanitation Councils (Committee on Drugs) and Central Social Insurance and Medical Councils (Chuikyo) are available as well.
Also, information about the Japanese Pharmacopoeia (JP), a collection of drug quality specifications, is available. Both Japanese and English PDF files are published for free.
Pharmaceuticals and Medical Devices Agency (PMDA)
This is the most important website for obtaining specific regulatory information about drugs.
The PMDA has 3 major responsibilities: reviews, post-marketing safety measures, and relief services for adverse health effects.
Of these, reviews and post-marketing safety measures are relevant to jobs at pharma companies.
Reviews are mostly focused on activities before product launch and post-marketing safety measures after product launch.
Packages inserts and review reports for approved drugs can be downloaded from this website.
Specific methods of downloading the documents are shown below.
Click on the button below on the top page.

In the next screen, place a name of the drug you are looking for.
Here we use Opdivo as an example to find its package insert and review report (This search system is only available in Japanese).

Make sure package inserts and review reports are checked.

After checking, click on the search button.

The resultant screen should be scrolled to the right, and click the links to the package insert and review report.

Also, the data summary of the approval application documents (or publicized CTD) can be viewed in the review report column.
US Food and Drug Administration (FDA)
This is obvious, but it is the American regulatory authority’s website that regulates drugs.
This FDA website conveys information, just like Japan’s PMDA website, regarding regulations or procedures necessary to launch a drug product in the US, as well as review and safety of drugs.
European Medicines Agency (EMA)
It is the regulatory authority of the European Union (EU).
This EMA website also conveys information, just like Japan’s PMDA website, regarding regulations or procedures necessary to launch a drug product in the EU, as well as review and safety of drugs.
Industry group websites
Federation of Pharmaceutical Manufacturer's Association of Japan (FPMAJ)
It is a group of the industry groups each consisting of pharma-companies.
FPMAJ consists of both business type-based industry groups like JPMA and area type-based industry groups like KPIA and PMAT.
Japan Pharmaceutical Manufacturers Association (JPMA)
An industry group consisting of research-oriented pharma companies.
The article, Pharmaceutical Regulations in Japan are publicized every year and available for free (in both Japanese and English).
Kansai Pharmaceutical Industry Association (KPIA)
An industry group consisting of Kansai-based pharma companies, which is previously called Osaka Pharmaceutical Industry Association (OPIA).
This group is more influential than PMAT because the pharma industry in Japan developed in Dosho-machi in Osaka and thus many pharma companies were Kansai-based.
The web-based database of notifications from the regulatory authorities, praise-net, which is only available for pharma companies belonging to the industry-groups, is a must tool for industry people.
Pharmaceutical Manufacturers’ Association of Tokyo (PMAT)
An industry group consisting of Tokyo-based pharma companies.
Literature searching websites
PubMed
This is a database for life science and medical literature, which is provided by the US National Library of Medicine. A service of choice for researching on literature in English.
Igaku Chuo Zasshi(Ichushi)
PubMed mentioned above does not cover Japanese literature.
When it comes to searching for medical literature in Japanese, this will be the service of choice. Registration with fees is required.
Other web resources
Medical Dictionary for Regulatory Activities (MedDRA)
Developed via ICH activities to meet the needs of regulatory authorities and pharma companies about a mutual medical dictionary.
Originally, based on glossaries used by the UK regulatory authority, Medicines and Healthcare products Agency (MHRA).
MedDRA can be available for free for non-commercial purposes, but for Japanese translation terms, registration with fees to the Japan Maintenance Organization is necessary.
Books
Drug Approval and Licensing Procedures in Japan
A book almost completely covers drug regulations and procedures in Japan, which is prepared by people in the industry groups and published by Jiho Inc.
Industry news
Daily Yakugyo
Daily news published by Jiho Inc., which is a publisher of books such as Drug Approval and Licensing Procedures in Japan and Therapeutics Handbook that everyone in the industry knows.
Basically, this service requires a subscription with fees but a free registration allows you to read a certain number of non-free articles.
Yakuji News
Weekly industry news.
With Yakuji News-Net Day, a service for healthcare professionals and pharma companies, you can get latest news via email, and access a quick summary and past materials of Pharmaceutical Affairs and Food Sanitation Councils.
Mix
A useful monthly magazine with non news-based articles, but well-balanced articles from a marketing perspective about the industry trend evenly from the hospital, pharmacy, wholesale, and pharma company setting is useful.
Monthly Yakuji
This is also a monthly magazine published by Jiho Inc. like Daily Yakugyo.
The title says Yakuji (regulatory), but it is mostly focused on contents for pharmacists working at hospitals and pharmacies.
解説
専門用語は赤字、製薬必修フレーズを構成する言い回し(製薬必修表現)は青字とした。
専門用語
Central Social Insurance and Medical Council:中央社会保険医療協議会。通称「中医協」。薬価や診療報酬をなど医療保険関係のトピックを議論する厚労大臣の諮問機関。
Japanese Pharmacopoeia (JP):日本薬局方(日局)。医薬品の品質規格基準書。厚生労働大臣が薬事・食品衛生審議会の意見を聞いて定める。
safety measures:安全対策業務。PMDAの3大業務の内の一つ。医薬品等の市販後の安全性情報を収集・管理する。
relief services for adverse health effects:健康被害救済業務。PMDAの3大業務の内の一つ。医薬品を適正に使用したにも関わらず発生した健康被害の救済を図る。
data summary:資料概要。資料の概要であるが、古くはイロハ申請での概要。国際的に標準化された様式であるCTDが導入された後は、CTD Module 2を指す。
FDA:米国食品医薬品局。本文中の説明を参照。
EMA:欧州医薬品庁。本文中の説明を参照。
medical literature:医学文献。
ICH:International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use 医薬品規制調和国際会議。日米欧で医薬品規制を共通化するために発足し、活動してきた規制当局と業界からなる団体。現在は日米欧だけでなく幅広い国をメンバーに持つ。
用語については本サイトの用語集も適宜参照されたい。
製薬必修表現
publicized:公開された。
a service of choice:第一選択となるサービス。「A service of 名詞」で通常複数の選択肢の中から最優先に選択されるものに用いられる表現。医薬品の第一選択薬という表現にも使用可能。
when it comes to:「○○の場合は」と表現するために便利フレーズ。「when it comes to 名詞」で用いる。
hospital, pharmacy, wholesale, and pharma company setting:病院、薬局、卸及び製薬企業の現場。「医療現場」、「実臨床下」等の表現に便利なフレーズ。





